Lineas de Investigación
Etapas de formación en química de carbohidratos
La única generalización que existe en química de carbohidratos es que no existe ninguna generalización
Durante la realización de mi tesis doctoral escuche en varias ocasiones de mi director de tesis esta frase que resalta la dificultad de la química de unas moléculas que poseen un elevado número de grupos funcionales del mismo tipo, el grupo hidroxilo. Para entender su reactividad hace falta una mirada holística. Por ejemplo, la glucosa y la galactosa tan solo difieren en la configuración de uno de los centros asimétricos, pero este simple cambio afecta a la reactividad relativa de todos los grupos hidroxilo.
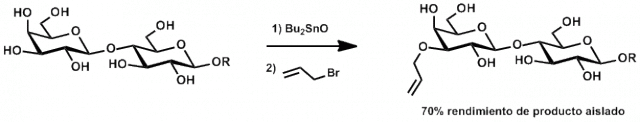
En la tesis se estudiaron reacciones de protección selectiva sobre la lactosa1-6 (Esquema 1), un disacárido compuesto precisamente de glucosa y galactosa. Se sintetizaron oligosacáridos fucosil-lactosas3 presentes en la leche humana, que confieren resistencia a infecciones en los lactantes alimentados con leche materna.
Como es habitual, el trabajo de tesis doctoral marcó la futura carrera investigadora. En etapas postdoctorales y en trabajos posteriores se han estudiado otras reacciones sobre carbohidratos y se han desarrollado estrategias de síntesis de oligosacáridos y análogos. Algunas de las más representativas serían:
- Reacción de eliminación reductora de tioglicósidos.7,8
- Reacciones de fosforilación y sintesis de fosfatos de inositol.9-11
- Síntesis de glicósidos y oligosacáridos de interés biológico.12-18, 23,24
- Síntesis de carbaazúcares, C-glicósidos y tioglicósidos, y estudios conformacionales alrededor del enlace glicosídico.19-22, 25,2
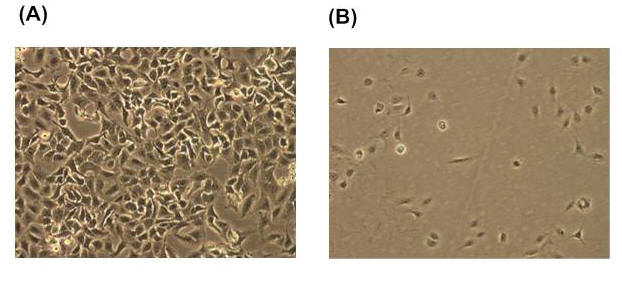
Glicósidos antitumorales
Cultivo de células tumorales en ausencia (A) y en presencia (B) de glicolípido sintético antitumoral.
La presencia de inhibidores de la división de células neurales en cerebro de ratas fue descrita por primera vez por el Prof. Manuel Nieto-Sampedro (Science 240 (1988) 1784-1786). Desde entonces y en colaboración con Nieto-Sampedro hemos trabajado en la elucidación estructural del inhibidor natural,6,9,15,17 y en la síntesis de moléculas más simples que portasen fragmentos estructurales del inhibidor.1-5,8,10,16,18 Hemos obtenido diversas generaciones de oligosacáridos complejos y glicósidos que se han ensayado como agentes antitumorales en cultivo y en animales. Hemos utilizado sistemas poliméricos para la administración controlada de los antitumorales.7-8,12-13 De entre todos los compuestos sintéticos el más activo ha resultado ser un glicósido del alcohol oleico (compuesto 1 en la Figura 1A). La conjugación del azúcar con alcohol oleico es fundamental para la actividad, pues otros alcoholes hidrocarbonados similares no fueron activos. Estudios sobre el mecanismo de acción revelaron que el glicósido produce cambios drásticos en los niveles de glicoesfingolípidos de las células tumorales e induce estrés del retículo endoplásmico, conduciendo finalmente a la muerte celular.11,14,16
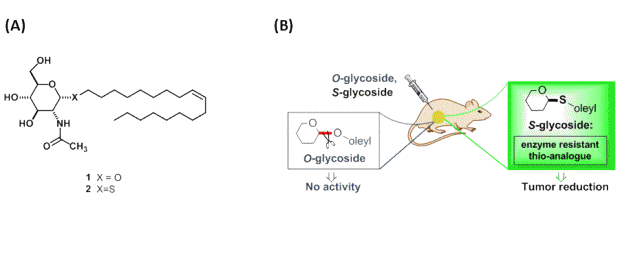
Figura 1.
Pese a los buenos resultados de 1, cuando se ensayó en ratas portadoras de un tumor cerebral, el compuesto fue inactivo. Con la ayuda de la RMN en estado sólido aplicando la técnica MAS pudimos comprobar que el compuesto era hidrolizado, probablemente por la acción de enzimas glicosidasas. Preparamos el análogo en el que el átomo de oxígeno en posición anomérica es reemplazado por un azufre (tioglicósido 2). El nuevo compuesto fue resistente a la hidrólisis enzimática y su empleo en animales condujo a una reducción significativa del tumor en comparación con los animales control (Figura 1B).16
Desde el laboratorio al paciente
Más del 70% de la población mundial es intolerante a la lactosa. La prueba del aliento, que es el método actualmente empleado para el diagnóstico de la intolerancia, es molesta para el paciente y poco fiable. Hemos desarrollado un nuevo método más directo y sencillo basado en el uso de un disacárido sintético.
En colaboración con el Prof. Juan José Aragón, de la Universidad Autónoma de Madrid, hemos desarrollado una nueva prueba diagnóstica de la intolerancia a la lactosa. El método es extremadamente sencillo, se basa en el uso de un disacárido, 4-galactosil-xilosa, que es obtenido mediante síntesis enzimática. El disacárido sintético es sustrato de la enzima lactasa intestinal, la cual lo hidroliza para dar lugar a los monosacáridos, galactosa y xilosa. La galactosa es metabolizada en el hígado mientras que la xilosa es absorbida pero no es metabolizada, siendo excretada en la orina (Figura 1). La medida de xilosa en orina o sangre nos informa de la actividad lactasa. A mayor cantidad de xilosa en orina o sangre, mayor es la actividad lactasa intestinal en el individuo.
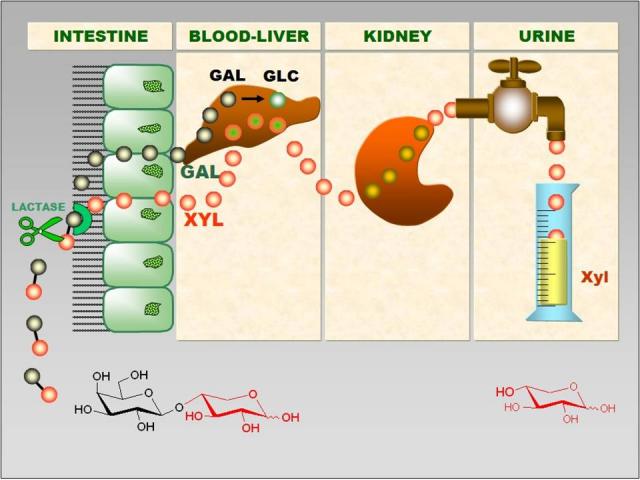
Figura 1.Esquema representativo del funcionamiento del nuevo test.
Con la finalidad de desarrollar y comercializar la prueba diagnóstica, fundamos la empresa LACTEST S.L. en 2003. Desde entonces hemos realizado los estudios preclínicos y clínicos necesarios para obtener información de la toxicidad, la farmacocinética y la eficacia del producto. También se ha realizado el escalado industrial del proceso de síntesis enzimática, el cual se lleva a cabo básicamente con el mismo procedimiento que pusimos a punto en el laboratorio. El producto se comercializa en España desde enero de 2013. Un proyecto que hemos desarrollado de principio a fin, desde la investigación en el laboratorio hasta su aplicación clínica.
Un ejemplo de colaboración entre grupos funcionales
A veces hay que tratar a los grupos funcionales como si fuesen niños: cuando no te dejan hacer una tarea porque incordian, lo más práctico es dejarles participar.
Con el fin de preparar oligosacáridos con actividad biológica que tengan enlaces de tipo tio-glicósido resistentes a la hidrólisis por enzimas glicosidasas, nos propusimos introducir un átomo de azufre en posición 3 de la N-acetilglucosamina por desplazamiento nucleófilo sobre la alosamina 1 (Esquema 1).1 Pero no fue trivial. El triflato no pudo formarse por culpa del grupo acetamido, que produjo reacciones secundarias como la formación de la oxazolina 2. El tosilato 3 pudo conseguirse pero resultó poco reactivo; igualmente sucedió con el grupo mesilato. Nos deshicimos del grupo acetamido transformándolo en un phthalamido. De este modo pudimos formar el triflato 4, pero cuando se sometió al desplazamiento nucleófilo dio lugar a una reacción de eliminación (producto 5). Después de otros intentos infructuosos y hartos de no saber qué hacer con el grupo acetamido, se nos ocurrió usarlo para formar junto con el alcohol un sulfamidato cíclico 6. La apertura regioselectiva de este grupo por nucleófilos transcurrió suave- y eficientemente, permitiéndonos introducir grupos funcionales en la posición deseada.1-4
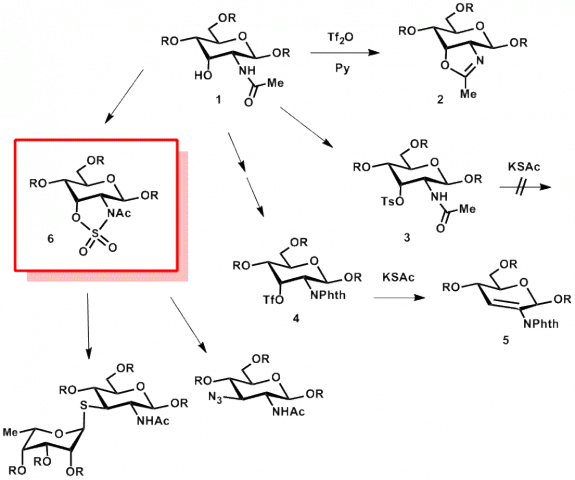
Esquema 1
Un caballo de Troya para la dopamina
La unión de una molécula con actividad farmacológica a otra molécula capaz de ser transportada a través de una barrera natural, podría dar lugar a un caballo de Troya molecular. Esta estrategia se ha estudiado frecuentemente con el fin de conseguir fármacos más eficaces.
El cerebro es el órgano más sensible y a la vez más vital de nuestro organismo. El paso de sustancias desde el torrente sanguíneo al cerebro está fuertemente restringido por la barrera hematoencefálica (BHE), que actúa como un filtro. La presencia de la BHE, sin embargo, es un inconveniente para el tratamiento de las enfermedades del sistema nerviosos central. Así, la enfermedad de Parkinson, que es causada por una disminución de los niveles de dopamina en el cerebro, no puede tratarse mediante la administración de dopamina pues este neurotransmisor no atraviesa la BHE.
Hemos estudiado una nueva aproximación para hacer llegar dopamina al cerebro basada en la utilización de derivados glucosilados de dopamina.1-3 La glucosa es el nutriente principal del cerebro, su consumo representa el 20-30% de la cantidad total de glucosa consumida por el organismo. Al ser tan necesaria, el paso de glucosa de la sangre al cerebro tiene lugar mediante el transportador de glucosa GLUT-1, que se encuentra sobreexpresado en la BHE. La hipótesis de trabajo suponía que la glucosa actuase como vector para hacer llegar dopamina al cerebro.
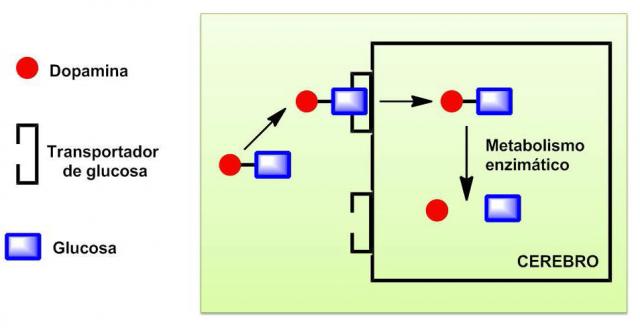
Se prepararon diversos derivados en los que la dopamina se une a distintos hidroxilos de la glucosa con diferentes grupos funcionales actuando como conectores. El estudio de transporte se realizó usando eritrocitos que expresan en su membrana el mismo transportador GLUT-1 que el presente en la BHE. La incorporación de los compuestos al interior de la célula se analizó por RMN en estado sólido aplicando la técnica MAS, que permite trabajar con células intactas, en combinación con inhibidores irreversibles del transportador.3 Los resultados indicaron que algunos derivados, los menos polares, se incorporaron al interior de la célula, pero en ningún caso mediante un transporte facilitado por el GLUT-1. Pese a todo, los trabajos proporcionaron resultados interesantes de estructura/afinidad por GLUT-1. Así, los derivados de glucosa con la sustitución en posición O-6 presentaron la mejor afinidad por GLUT-1, algunos de ellos se unieron más eficientemente al transportador que la glucosa misma.2 Al no ser luego transportados al interior de la célula, se portan como inhibidores del transporte de glucosa. El trabajo también puso de manifiesto la dificultad de emplear transportadores específicos para vehiculizar fármacos.
Organocatálisis en la síntesis de derivados de azúcares
La organocatálisis se define como la catálisis por pequeñas moléculas orgánicas como, por ejemplo, aminoácidos. La presencia de aminoácidos asimétricos en meteoritos carbonáceos ha llevado a proponer que otros elementos prebióticos , como son los azúcares, hayan podido generarse mediante una adición organocatalizada de glicolaldehído y formaldehido.
Sin llegar a tanto, mediante el empleo de la catálisis con el aminoácido prolina hemos descrito una estrategia de obtención de iminoazúcares. Estos compuestos presentan el oxígeno del anillo de piranosa reemplazado por un átomo de nitrógeno y poseen una fuerte actividad como inhibidores de glicosidasas. La estrategia implica una reacción de adición aldólica entre un aldehído proveniente del tartrato y una cetona, catalizada por prolina.2 Es altamente versátil puesto que en función de la configuración del tartrato de partida y de la prolina podemos obtener diferentes iminoazúcares (Esquema 1). La estereoselectividad de la reacción aldólica se estudió mediante modelización molecular.4
Hemos estudiado la reacción aldólica con prolina inmovilizada en material mesoporoso MCM41, lo que permite recuperar y reutilizar el catalizador. Con la catálisis heterogénea es posible llevar a cabo la reacción en diferentes disolventes orgánicos, incluidos los más hidrófobos como tolueno.1,3
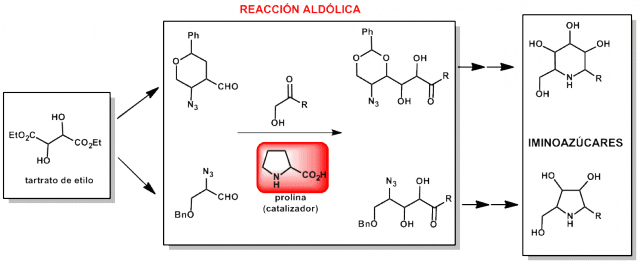
Esquema 1.Ruta de síntesis de iminoazúcares con anillos de 5 y 6 miembros.
OrgaCatalizadores políméricos a partir de sus monómeros
La obtención de catalizadores poliméricos a partir de sus monómeros permite una flexibilidad en el diseño superior al método más convencional de unir el catalizador a un soporte prefabricado.
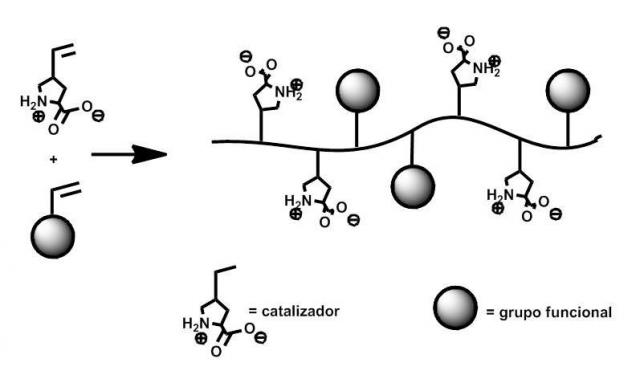
Los catalizadores soportados en polímeros orgánicos son de gran interés en síntesis orgánica por la posibilidad que brindan de recuperarse fácilmente y reutilizarse. Lo habitual es utilizar soportes prefabricados (por ejemplo, las resinas de estireno en catálisis heterogénea o el polietilenglicol en catálisis homogénea), los cuales son modificados químicamente para introducir el catalizador. Hemos descrito por primera vez la síntesis de polímeros lineales de prolina a partir de sus monómeros para su empleo en reacciones aldólicas en agua. Esta estrategia ofrece una flexibilidad en el diseño del catalizador superior al uso de polímeros prefabricados. Así, a partir de metacrilatos derivados de prolina hemos obtenido polímeros a los que hemos incrementado gradualmente su carácter hidrofóbico (lo cual mejoró progresivamente su actividad catalítica en agua) mediante copolimerización con estireno. O bien, hemos introducido un anillo de ciclodextrina con capacidad de complejar moléculas orgánicas. De tal modo que el polímero resultante podría mimetizar una enzima aldolasa, con un centro catalítico (la prolina) y un bolsillo hidrofóbico (la cavidad de la ciclodextrina). Pudo observarse con algunos polimeros que la adición de cloruro magnésico o cambios en el pH conduce a la formación de nanoagregados de las cadenas poliméricas lo que produce un incremento muy significativo de la estereoselectividad de la reacción.
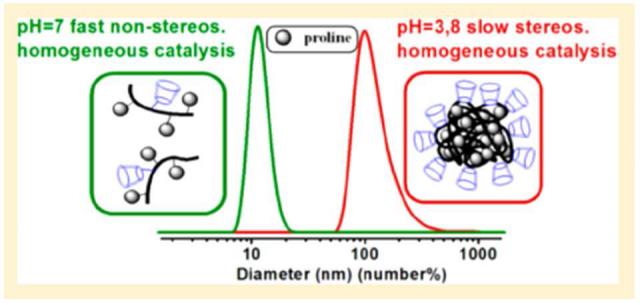
Esta estrategia abre un campo de posibilidades en el diseño de catalizadores poliméricos. Así, además de introducir sitios de unión del sustrato, se puede pensar, por ejemplo, en introducir un cocatalizador u otro grupo catalítico complementario que permita llevar a cabo reacciones consecutivas en las que el producto de una reacción sea el reactivo de la siguiente. También se puede pensar en el diseño de polímeros lineales que formen nanoagregados estructurados en agua con un compartimento que actúe como centro activo, lo cual sería un ejemplo de convergencia de la química macromolecular y la química supramolecular.
Nuevos materiales para la regeneración del tejido nervioso
En la actualidad estamos iniciando un proyecto en colaboración con el Hospital Nacional de Parapléjicos de Toledo dirigido al tratamiento de las lesiones medulares.